干细胞治疗肌肉萎缩的重大新发现
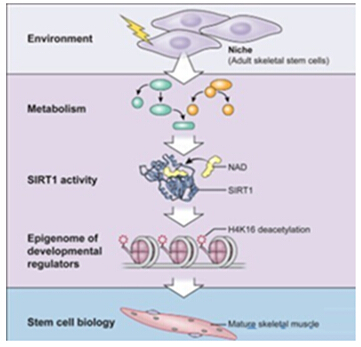
近日,来自美国NIH的Vittorio Sartorelli研究小组发现,在骨骼肌干细胞中,Sirt1能够感受代谢变化信号并通过其去乙酰化酶活性影响H4K16乙酰化修饰,启动肌肉基因表达转录,NAD+依赖性去乙酰化酶Sirt1已经被发现在许多生物学过程中都发挥重要作用。这一研究成果发表在干细胞领域顶尖期刊Cell stem cell上。
研究人员发现,在生长条件良好的培养环境中,处于静止期的骨骼肌干细胞代谢会经历从脂肪酸和丙酮酸氧化向糖酵解方向的转化,并且激活戊糖磷酸途径合成许多代谢小分子。同时,相比于激活的骨骼肌干细胞,静止期细胞中sirt1的去乙酰化酶活性和NAD+水平更高,因此,当静止期细胞代谢方向改变,细胞中NAD+水平下降,sirt1的去乙酰化酶活性随之降低,导致组蛋白H4K16乙酰化水平增高,启动骨骼肌分化相关基因的表达。研究人员通过构建sirt1在骨骼肌细胞特异性敲除的小鼠模型,发现sirt1功能缺失会导致敲除小鼠骨骼肌细胞出现纺锤样瘦长形态,说明敲除小鼠体内骨骼肌细胞同样出现了过早分化。
细胞通过胞质内的糖酵解和线粒体内氧化磷酸化产生能量,细胞代谢除了提供稳定的能量供应,还会影响表观基因组,改变基因表达。当氧气供应降低,细胞通过无氧糖酵解合成ATP,而在有氧条件下,ATP的合成主要通过氧化磷酸化来进行,这一过程会导致细胞内NAD+含量增加。Sirt1属于III类去乙酰化酶家族,它能够通过NAD+感受细胞能量代谢变化,并通过其去乙酰化酶活性影响底物的乙酰化水平,将代谢信号转化为表观遗传信号,影响细胞基因表达。
综上所述,该文章发现骨骼肌干细胞能够通过sirt1感受细胞能量代谢变化,并且以表观遗传修饰的方式影响骨骼肌干细胞向成熟骨骼肌细胞分化过程。了解这一过程对治疗肌肉萎缩等肌肉相关疾病具有重要意义。




 400-817-8855
400-817-8855 预约咨询
预约咨询
